Page 391 - Wireman - TP - Hindi
P. 391
जहाँ Z = इयतु सेल का कार (Type of cells)
फै राडे के इले ोिलिसस के िनयमों के अनुसार सेल (Cell): एक सेल एक िवद् त रासायिनक उपकरण है िजसम िविभ
सामि यों से बने दो इले ोड और एक इले ोलाइट होता है। इले ोड
m = Z . I . t
और इले ोलाइट के बीच रासायिनक िति या एक वो ेज उ करती
जहाँ, m = मु पदाथ का ाम म मान है।
z = ाम म पदाथ का िवद् त रासायिनक समतु सेल को वग कृ त िकया गया है
i = ए ीयर म करंट • शु सेल
t = सेकं ड म समय • गीली सेल
नोट: जमा िकया गया मान m = आयतन x घन एक शु सेल वह होता है िजसम पे या जेल इले ोलाइट होता है। नए
िडजाइन और िनमा ण तकनीकों के साथ, यह संभव है।
ाथिमक सेल (Primary cells): ाथिमक सेल वे सेल होते ह जो
रचाज बल नहीं होते ह । यानी िड चाज के दौरान होने वाली रासायिनक
िति या उलटी नहीं होती है। जब सेल पूरी तरह से िड चाज हो जाता है तो
त ों के इले ो-रासायिनक समतु के िलए टेबल िति याओं म उपयोग िकए जाने वाले सभी रसायन प रवित त हो जाते ह ।
त का परमा क संयोजकता इले ो- रासायिनक इसके बाद इसे एक नए सेल ारा ित थािपत िकया जाना चािहए।
नाम भार के िमकल समक
ाथिमक सेल के कार (Types of primary cells ):
समतु
• वो ाइक सेल
mg/c
हाइड ोजन 1.008 1 0.01045 1.008 • काब न-िजंक सेल (ले ांच सेल और ड ाई सेल)
अ ुमीिनयम 27.1 3 0.0936 9.03 • ारीय सेल
ताँबा 63.57 2 0.3293 31.78 • मक री सेल
चाँदी 107.88 1 1.118 107.88 • िस र ऑ ाइड सेल
ज ा 65.38 2 0.3387 32.69 • िलिथयम सेल
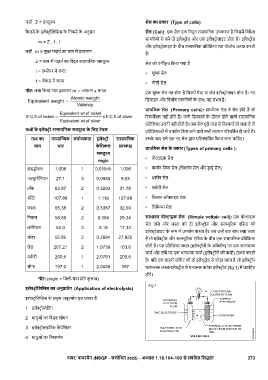
िनकल 58.68 2 0.304 29.34 साधारण वो ाइक सेल (Simple voltaic cell): एक वो ाइक
सेल तांबे और ज ा को दो इले ोड और स ू रक एिसड को
ोिमयम 52.0 3 0.18 17.33
इले ोलाइट के प म उपयोग करता है। जब उ एक साथ रखा जाता
लोहा 55.85 2 0.2894 27.925 है तो इले ोड और स ू रक एिसड के बीच एक रासायिनक िति या
लेड 207.21 2 1.0738 103.6 होती है। यह िति या ज ा (इले ॉनों के अिधशेष) पर एक ऋणा क
चाज और तांबे पर एक धना क चाज (इले ॉनों की कमी) उ करती
मक री 200.6 1 2.0791 200.6
है। यिद एक बाहरी सिक ट को दो इले ोड से जोड़ा जाता है, तो इले ॉन
सोना 197.0 1 2.0438 197 ऋणा क ज ा इले ोड से धना क कॉपर इले ोड (fig 1) म वािहत
होंगे।
नोट: (mg/c = िमली- ाम ित कू ल )
Fig 1
इले ोिलिसस का अनु योग (Application of electrolysis)
इले ोिलिसस के मुख अनु योग इस कार ह :
1 इले ो ेिटंग
2 धातुओं का िवद् त शोधन
3 इले ोलाइिटक कै पेिसटर
4 धातुओं का िन ष ण
पावर: वायरमैन (NSQF - संशोिधत 2022) - अ ास 1.18.104-109 से संबंिधत िस ांत 373